Nifuroksazid (NFZ) (Şekil 1), Laboratoires Robert & Carriere SA (Fransa) tarafından 1961 yılında Fransa’da ve 1966 yılında ABD’de patenti alınan bir gastrointestinal antibakteriyel ajandır. İlaç, 1970’lerde yaygın olarak kullanılmış ve yoğun bir şekilde tanıtılmıştır. NFZ ilk olarak bakteriyel vajinit, Chlamydia trachomatis, Mycoplasma ve Candida enfeksiyonlarının etkili ve güvenli tedavisi için geniş spektrumlu bir bağırsak antiseptiği olarak tanımlanmıştır.
Kandaki konsantrasyonuna bağlı olarak, NFZ bakteriyostatik veya bakterisidal etki gösterir ve öncelikle akut, enfeksiyöz ishal tedavisinde kullanılır. Bağırsak enfeksiyonlarının etkenlerinin çoğuna karşı etkilidir: Gram pozitif (Staphylococcus ailesi) ve Gram negatif (Enterobacteriaceae ailesi: Escherichia, Citrobacter, Enterobacter, Klebsiella, Salmonella, Shigella, Yersinia) ve ayrıca Vibria cholerae. Ancak Pseudomonas ve Proteus‘a karşı etkisizdir. NFZ esas olarak enfeksiyöz kolit ve ishal tedavisinde kullanılır, ancak diğer ilaçlarla, örneğin kabızlığın tedavisi için Plantago ovata musilajı ile birlikte de kullanılabilir.
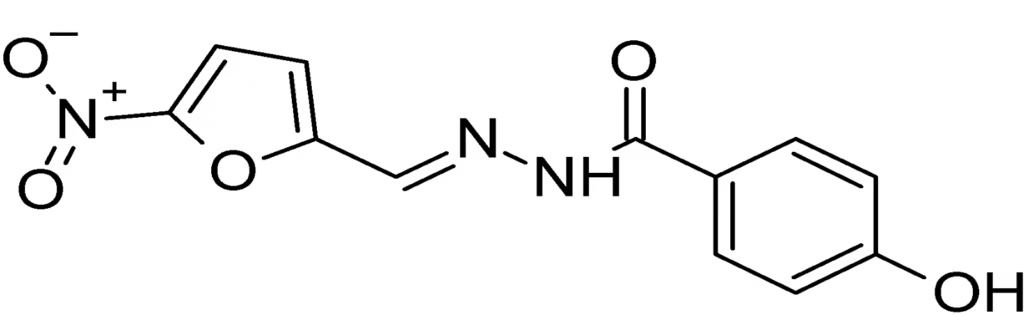
Şekil 1. Nifuroksazid: 4-Hidroksi-N-[(E)-(5-nitrofuran-2-il)metilidenamino]benzamit.
NFZ yapısı, aromatik hidrazit-hidrazonların geniş bir sınıfının temsilcisi olan 5-nitro-2-furaldehit 4-hidroksibenzhidrazondur. Ağızdan alındığında, ilaç karaciğerde metabolize edilebilir. NFZ iyi tolere edilir, ancak sindirim sürecinde bozulma ve sonunda deri döküntüsü, ürtiker, anjiyoödem (ve nadir görülen ciddi immün-alerjik reaksiyonlar ve anafilaktik şok vakaları) gibi alerjik reaksiyonlar şeklinde ara sıra yan etkiler görülebilir. NFZ’in memeli hücrelerinde mutajenik olduğu düşünülmüştür.
NFZ’nin uzun bir klinik uygulama geçmişi olup 2008 yılında Prestwick kütüphanesindeki 1.200 biyoaktif bileşiğin taranmasıyla sinyal iletimi ve transkripsiyonel aktivasyon faktörü 3 (STAT3) bağımlı gen ekspresyonunun güçlü bir inhibitörü olarak tanımlanmıştır. Son çalışmalar, NFZ’nin belirgin anti-tümör etkilerine sahip olduğunu göstermiş ve antikanser aktivitesi üzerine çok sayıda çalışma yürütülmüştür.
STAT3, sitoplazmik indüklenebilir bir transkripsiyon faktörüdür ve genellikle sitokinler veya interlökin-6 (IL-6) veya epidermal büyüme faktörü (EGF) gibi büyüme faktörleri tarafından sağlanan hücre dışı sinyalleri iletir. STAT3 aktivasyonuna yol açan temel sinyal yolu, IL-6’nın bir sitokin reseptörü tarafından tanınmasını, ardından ilişkili Janus tirozin kinazların (JAK’lar) aktivasyonunu, sitoplazmik STAT3’ün JAK tarafından fosforilasyonunu ve fosforile edilmiş STAT3’ün çekirdeğe taşınmasını içerir ve burada gen ekspresyonunu düzenler. STAT3 ise, onkojenezde önemli bir risk faktörü olan kronik inflamasyonu desteklediği bilinen bir dizi sitokin, kemokin ve diğer faktörlerin ekspresyonunu tetikler.
STAT3, kanser proliferasyonu, invazyonu ve metastazında rol oynayan bir dizi geni yukarı düzenler. Bu transkripsiyon faktörünün kanser hücresi bağışıklık sisteminden kaçışındaki rolü de kabul edilmiştir. Bu nedenle, JAK/STAT3 yolunu hedeflemek, kanser immünoterapilerinde potansiyel olarak önemli bir yaklaşım olarak belirlenmiş ve yolu inhibe eden ajanların geliştirilmesine önemli bir çaba harcanmıştır. JAK2’nin doğrudan etkili inhibitörleri ruksolitinib ve fedratinib, bazı lösemilerin tedavisi için FDA tarafından onaylanmıştır; buna karşın birkaç düzine daha JAK ve STAT3 inhibitörü çeşitli kanserlere karşı klinik denemelerden geçmektedir. Ayrıca, şu anda klinik kullanımda olan bir dizi ilacın, kanserde JAK/STAT3 yolunun inhibitörleri olarak tanımlanmıştır. Örneğin, enfeksiyöz ishallerin tedavisinde kullanılan sentetik bir antibakteriyel olan NFZ, 15 yıl önce STAT3’ün güçlü bir inhibitörü olarak tanımlanmıştır ve deneysel melanom, pulmoner fibroz, hepatoselüler karsinom ve diyabetik böbrek hastalığındaki inflamatuar durumlara karşı etkilidir.
STAT3, birden fazla onkojenik sinyal yolunun birleşme noktasıdır ve çeşitli insan kanserlerinde yapısal olarak aktiftir. Özellikle STAT3, meme tümörlerinin %70’inde, özellikle üçlü negatif tümörlerde aktive olur. Bu temelde, Yang ve arkadaşları, NFZ’nin doza bağlı olarak proliferasyonu inhibe ettiğini, apoptozu indüklediğini ve meme kanseri hücrelerinin göçünü ve invazyonunu kısıtladığını göstermiştir. En önemlisi, ilacın in vivo olarak meme tümörü büyümesini ve akciğer metastazını azalttığı gösterilmiştir. NFZ ayrıca, önemli bir toksisite olmaksızın akciğerdeki miyeloid kaynaklı baskılayıcı hücrelerin infiltrasyonunu da azaltmıştır.
NFZ’nin ayrıca kanser hücresi apoptozunu indüklediği ve tümör büyümesini engellediği gösterilmiştir. Son zamanlarda, NFZ’in, ALDH yüksek kanser başlatıcı hücreleri seçici olarak öldüren güçlü bir aldehit dehidrojenaz (ALDH1) inhibitörü olduğu tanımlanmıştır. Bu iki çığır açan keşif, “STAT3 ve ALDH1 inhibisyonu” NFZ’nin hedefli bir antikanser ajan olarak yeniden konumlandırılma potansiyelini güçlü bir şekilde desteklemektedir (Şekil 2).
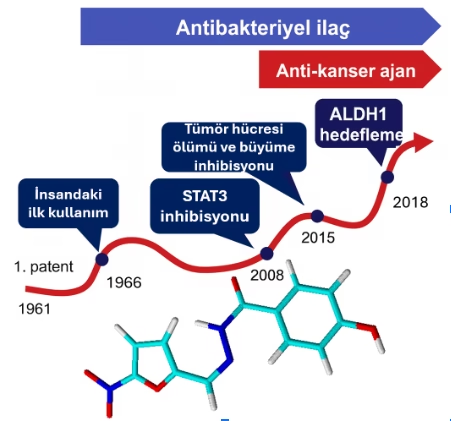
Şekil 2. Nifuroksazid’in keşfi ve yeniden konumlandırma süreçleri.
KAYNAKLAR
- Bailly C. Toward a repositioning of the antibacterial drug nifuroxazide for cancer treatment. Drug Discov Today. 2019;24(9):1930-1936.
- Mossine VV, Kelley SP, Waters JK, Mawhinney TP. Screening a small hydrazide-hydrazone combinatorial library for targeting the STAT3 in monocyte-macrophages with insulated reporter transposons. Medicinal Chemistry Research. 2023;32:682–693.
- Liu L, Ma C, Ji J, Gao R, Li D. Role of antidiarrheal agents nifuroxazide in antitumor multi-target anticancer, multi-mechanism anticancer drug. Oncol Lett. 2025;29(6):260.










